对于制造业,尤其是汽车供应链和医疗器械行业的企业而言,获取国际公认的质量管理体系认证是进入核心市场、提升管理水平和增强客户信任的关键步骤。本文将分别阐述在惠州地区备受关注的IATF 16949认证的基本核心内容,以及为广州及周边地区企业提供一份详实的ISO 13485认证文件参考清单,以助力企业高效开展认证咨询与准备工作。
第一部分:惠州IATF 16949认证基本内容解读
IATF 16949是国际汽车工作组制定的汽车行业质量体系标准,它基于ISO 9001,但增加了汽车行业的特殊要求。其基本内容与核心思想主要体现在以下几个方面:
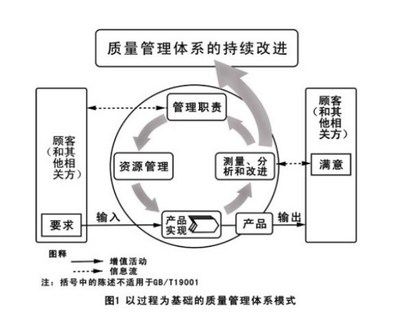
- 核心基础——过程方法:标准要求企业识别并管理相互关联的各类过程(如管理职责、资源管理、产品实现、测量分析与改进),强调过程的输入、输出、绩效指标及持续改进。
- 风险思维:将基于风险的思维贯穿于整个体系,要求组织识别可能影响体系、过程及产品和服务符合性的风险与机遇,并采取相应措施。
- 汽车行业特定要求:这是IATF 16949的精髓,主要包括:
- 产品安全:对可能影响安全的产品和过程提出严格要求,确保在整个供应链中传递。
- 供应商质量管理:对供应商的选择、绩效监控与开发提出了系统且严格的规定。
- 变更管理:对产品、过程及供应链的任何变更,都必须进行系统的控制与验证。
- 追溯性:要求建立从原材料到成品交付的完整追溯系统。
- 制造过程能力:强调对生产过程的统计控制(如SPC),确保稳定性和能力指数(如Cpk)。
- 顾客特殊要求(CSR):必须识别并满足直接顾客(如整车厂)的特定要求。
- 五大核心工具的应用:标准明确要求有效应用APQP(产品质量先期策划)、PPAP(生产件批准程序)、FMEA(潜在失效模式及后果分析)、SPC(统计过程控制)和MSA(测量系统分析),这些是体系有效运行的重要支撑。
对于惠州地区的汽车零部件企业而言,深入理解并落实这些内容,是成功通过认证、融入全球汽车供应链的基石。
第二部分:广州ISO 13485认证文件参考清单
ISO 13485是医疗器械质量管理体系的专用标准,其文件化信息要求是体系建立和审核的重点。以下是一份为准备认证(尤其适用于广州及华南地区医疗器械研发、生产、经营企业)的通用文件参考清单:
一、 体系层面文件
1. 质量手册:描述整个质量管理体系的范围、过程及其相互作用。
2. 程序文件:覆盖标准主要要求的形成文件的程序,例如:
* 文件控制程序
- 记录控制程序
- 管理评审控制程序
- 人力资源控制程序
- 基础设施与工作环境控制程序
- 风险管理程序(至关重要)
- 设计和开发控制程序
- 采购控制程序
- 生产和服务提供控制程序(含清洁、灭菌、产品防护等特殊过程)
- 监视和测量设备控制程序
- 顾客反馈处理与投诉处理程序
- 不合格品控制程序
- 数据分析与改进控制程序(含纠正和预防措施)
二、 技术与管理记录(关键证据)
1. 管理职责类:质量方针、目标及达成情况统计,管理评审计划、记录与报告,组织结构与职责权限规定。
2. 资源管理类:人员资质档案、培训计划与记录,设备清单、维护保养记录,工作环境监控记录。
3. 产品实现类:
* 设计与开发:设计开发计划、输入、评审、验证、确认、转换及更改的全部记录。
- 采购:合格供应商名录、评价记录、采购合同/订单、进货检验记录。
- 生产:工艺文件、作业指导书、批生产记录、过程检验记录、环境监测记录(如洁净车间)、灭菌验证报告(如适用)、产品标识与追溯记录。
- 测量、分析与改进类:产品出厂检验规程与报告、内部审核计划与报告、顾客反馈与投诉处理记录、不合格品处理记录、纠正/预防措施报告、数据分析报告(如不良率统计)。
- 法规与标准专有文件:医疗器械产品注册证/备案凭证、产品技术要求、符合性声明、临床评价报告(如适用)、上市后监督计划与报告、UDI(唯一器械标识)实施记录。
三、 外部文件
适用的医疗器械法律法规(如中国《医疗器械监督管理条例》)、国家/行业标准、顾客要求等清单及文本。
认证咨询建议
无论是筹备IATF 16949还是ISO 13485认证,专业咨询都至关重要。建议企业:
- 选择专业机构:寻找在特定行业(汽车或医疗器械)有丰富成功案例和资深审核背景的咨询机构。
- 差距分析先行:让咨询师对企业现状进行系统诊断,识别与标准要求的差距,制定切实可行的推行计划。
- 全员参与培训:确保从管理层到执行层都能理解标准要求及其工作职责,尤其是核心工具(对IATF 16949)和风险管理(对ISO 13485)的培训。
- 注重体系实效:避免“两层皮”,将标准要求深度融合到实际业务运营中,真正提升管理效率和产品可靠性。
通过系统性地理解标准核心并准备完备的文件化信息,惠州和广州的企业能够更顺畅地通过认证审核,为企业的长远发展和市场开拓奠定坚实的管理基础。